Préserver l'intégrité des données grâce au logiciel GlobalVision

Cela peut sembler être un autre mot à la mode de l'industrie pharmaceutique et des sciences de la vie, mais « l'intégrité des données » est tout aussi importante que la validation des systèmes informatiques lors de la mise sur le marché des produits. Il s'étend au-delà des frontières de l'informatique et aide les entreprises à prendre les bonnes décisions sur la base des bonnes données.
La plateforme de contrôle qualité GlobalVision est utilisée par les entreprises des sciences de la vie du monde entier pour les aider à gérer les processus de qualité de l'étiquetage et de l'emballage et à détecter les erreurs. Le logiciel permet aux clients d'approuver des fichiers d'illustration PDF ou des composants imprimés en vue de leur mise sur le marché. En tant qu'élément essentiel du processus d'approbation des illustrations d'emballage, les exigences d'intégrité des données doivent être respectées pour s'assurer que les bonnes données sont approuvées.
L'intégrité des données nécessite l'assurance que tout ce qui est collecté est attribuable, lisible, enregistré simultanément, original et exact (ALCOA, selon la Food and Drug Administration). En d'autres termes, il doit être fiable et non altéré. Dans les industries axées sur les données, ce besoin est omniprésent. Les précautions appropriées doivent être prises.
Trois niveaux d'accès distincts
Lorsqu'il s'agit d'un logiciel d'inspection, le défi consiste à le valider pour s'assurer que les bons défauts sont détectés et non pas des faux positifs. Une fois ces paramètres déterminés, il est important qu'ils soient utilisés par les opérateurs sans modification. Dans GlobalVision, cela se fait par le biais de trois niveaux d'accès utilisateur distincts :
Utilisateur
Utilisateurs avec la valeur par défaut Utilisateur les niveaux d'accès sont autorisés à effectuer des inspections, à examiner et à vérifier les différences, à générer et à imprimer des rapports d'inspection et à modifier leur mot de passe.
Directeur
Les utilisateurs disposant du Directeur les niveaux d'accès sont en outre autorisés à personnaliser les niveaux de reporting et les commentaires, à créer et à gérer des flux de travail, à forcer la révision/l'inclusion de toutes les différences dans les rapports d'inspection, à gérer les profils d'inspection et les paramètres associés, et à demander des licences d'application supplémentaires.
Administrateur
Utilisateurs avec Administrateur access peut faire tout ce qui précède. Ils peuvent également gérer les comptes utilisateurs et les paramètres associés, modifier les mots de passe et consulter, imprimer et exporter des pistes d'audit.
Piste d'audit avec accès restreint
Chaque fois que des modifications sont apportées aux données, il est important de les saisir. Vous voulez pouvoir consulter l'historique des modifications apportées au système à tout moment.
Les pistes d'audit sont essentielles à la conservation des données intégrité car ils représentent un compte rendu sécurisé et indépendant de toutes les activités. Chaque action entreprise peut être retracée jusqu'à un utilisateur. Dans GlobalVision, les événements documentés capturent toutes les données critiques, des connexions et déconnexions aux modifications de paramètres individuels concernant les comptes utilisateurs et les paramètres d'inspection.
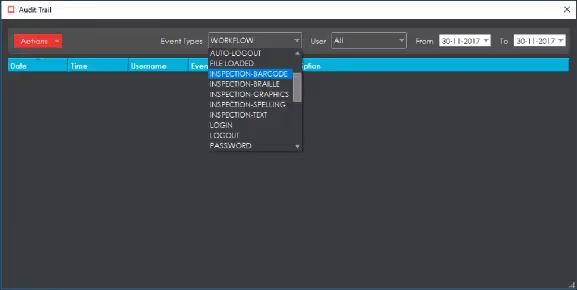
Rapports d'inspection
Les rapports d'inspection sont automatiquement stockés dans la base de données du logiciel dès leur génération et accessibles via l'Audit Trail. Cela ajoute une couche de protection supplémentaire importante, de sorte que vous pouvez toujours revenir au rapport d'inspection d'origine, au cas où des modifications seraient apportées en dehors du système GlobalVision.
Les rapports stockés dans la base de données ne sont pas de simples sauvegardes (autre caractéristique de l'intégrité des données). Ils constituent également une protection contre toute falsification hypothétique des rapports, au cas où les fichiers PDF téléchargés seraient modifiés de quelque manière que ce soit à l'aide d'outils tels qu'Adobe® Acrobat®.
Les originaux sont facilement disponibles pour référence ultérieure.
De leur côté, les rapports sont complets et détaillent clairement :
- Les noms des fichiers inspectés
- L'utilisateur qui les a inspectés
- Quand ils ont été inspectés
- Différences classées et commentaires
- Résumé des différences inclues/exclues
- Profils d'inspection utilisés
- Tous les paramètres d'inspection associés

Le rapport fournit une traçabilité complète sur quoi, qui, quand un produit a été inspecté et les données relatives aux paramètres d'inspection. L'inspection complète peut ensuite être reproduite à tout moment.
Conclusion
La FDA exige le 21 CFR Part 11 conformité pour les enregistrements électroniques. Au fil des ans, cela s'est étendu du simple stockage des données dans une piste d'audit à la vérification de l'exactitude des données stockées dans les applications et dans la piste d'audit. Développée selon les exigences les plus strictes en matière d'intégrité des données pharmaceutiques, chaque version de GlobalVision suit en outre un cycle de développement logiciel complet, garantissant ainsi le respect, la conception, le développement et les tests des exigences fonctionnelles en matière de pistes d'audit et d'intégrité des données.
GlobalVision protège contre les erreurs d'emballage qui affectent les clients qui achètent des produits hors des rayons des magasins. C'est essentiel, sans aucun doute. Cependant, les mesures d'urgence intégrées protègent également les organisations qui utilisent le logiciel en garantissant que les données ne sont jamais perdues. Il reste disponible pour ceux qui pourraient en avoir besoin. Plus important encore, il reste totalement inchangé.


