Aufrechterhaltung der Datenintegrität mit der GlobalVision-Software

Es mag wie ein weiteres Schlagwort der Pharma- und Life-Sciences-Branche klingen, aber „Datenintegrität“ ist genauso wichtig wie die Validierung von Computersystemen, wenn Produkte auf den Markt gebracht werden. Sie reicht über die Grenzen der IT hinaus und hilft Unternehmen, auf der Grundlage der richtigen Daten die richtigen Entscheidungen zu treffen.
Die GlobalVision Quality Control Platform wird von Life-Science-Unternehmen auf der ganzen Welt verwendet, um Qualitätsprozesse bei der Etikettierung und Verpackung zu verwalten und Fehler zu finden. Die Software ermöglicht es Kunden, PDF-Grafikdateien oder gedruckte Komponenten für die Markteinführung zu genehmigen. Da es sich um einen wichtigen Teil des Genehmigungsprozesses für Verpackungskunstwerke handelt, müssen die Anforderungen an die Datenintegrität erfüllt werden, um sicherzustellen, dass die richtigen Daten genehmigt werden.
Datenintegrität erfordert die Zusicherung, dass alles, was gesammelt wird, zuordenbar, lesbar, gleichzeitig aufgezeichnet, originell und korrekt ist (ALCOA, laut der Food and Drug Administration). Mit anderen Worten, es muss zuverlässig und unverfälscht sein. In datengesteuerten Branchen ist dieser Bedarf allgegenwärtig. Es müssen angemessene Vorsichtsmaßnahmen getroffen werden.
Drei separate Zugriffsebenen
Die Herausforderung bei Inspektionssoftware besteht darin, sie zu validieren, um sicherzustellen, dass die richtigen Fehler gefunden werden und keine Fehlalarme. Sobald diese Einstellungen festgelegt sind, ist es wichtig, dass sie von den Bedienern unverändert verwendet werden können. In GlobalVision wird dies durch drei separate Benutzerzugriffsebenen erreicht:
Nutzer
Benutzer mit der Standardeinstellung Nutzer Zugriffsebenen sind berechtigt, Inspektionen durchzuführen, Unterschiede zu überprüfen und nachzuweisen, Inspektionsberichte zu erstellen und auszudrucken und ihr Passwort zu ändern.
Geschäftsführer
Benutzer mit dem Geschäftsführer Zugriffsebenen sind außerdem berechtigt, Berichtsstufen und Kommentare anzupassen, Workflows zu erstellen und zu verwalten, die Überprüfung/Aufnahme aller Unterschiede in Inspektionsberichten zu erzwingen, Inspektionsprofile und zugehörige Parameter zu verwalten und zusätzliche Anwendungslizenzen anzufordern.
Administrator
Nutzer mit Admin Access kann all das tun. Sie können auch Benutzerkonten und zugehörige Einstellungen verwalten, Passwörter ändern und Prüfprotokolle anzeigen, drucken und exportieren.
Audit-Trail mit eingeschränktem Zugriff
Immer wenn sich Daten ändern, ist es wichtig, diese zu erfassen. Sie möchten jederzeit den Verlauf der Änderungen im System einsehen können.
Audit-Trails sind der Schlüssel zur Datenpflege Integrität, da sie eine sichere, unabhängige Abrechnung aller Aktivitäten darstellen. Jede durchgeführte Aktion kann auf einen Benutzer zurückgeführt werden. In GlobalVision erfassen dokumentierte Ereignisse alle wichtigen Daten, von An- und Abmeldungen bis hin zu individuellen Einstellungsänderungen in Bezug auf Benutzerkonten und Inspektionsparameter.
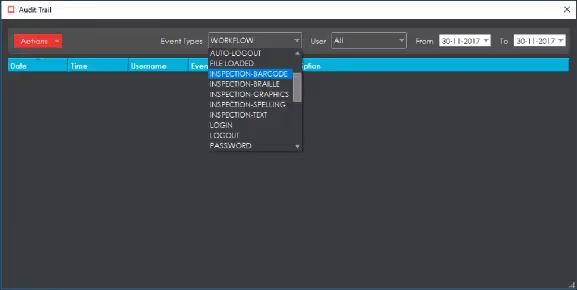
Inspektionsberichte
Inspektionsberichte werden nach ihrer Generierung automatisch in der Datenbank der Software gespeichert und sind über den Audit Trail zugänglich. Dies bietet eine wichtige, zusätzliche Schutzebene, sodass Sie jederzeit zum ursprünglichen Inspektionsbericht zurückkehren können, falls Änderungen außerhalb des GlobalVision-Systems vorgenommen werden.
In der Datenbank gespeicherte Berichte dienen mehr als bloße Backups (ein weiteres Kennzeichen der Datenintegrität). Sie schützen auch vor hypothetischen Manipulationen an Berichten, falls die heruntergeladenen PDF-Dateien in irgendeiner Weise mit Tools wie Adobe® Acrobat® verändert werden sollten.
Die Originale sind zum späteren Nachschlagen leicht verfügbar.
Die Berichte sind ihrerseits umfassend und detailliert:
- Die Namen der inspizierten Dateien
- Der Benutzer, der sie überprüft hat
- Als sie inspiziert wurden
- Kategorisierte Unterschiede und Kommentare
- Zusammenfassung der eingeschlossenen/ausgeschlossenen Unterschiede
- Verwendete Inspektionsprofile
- Alle zugehörigen Inspektionsparameter

Der Bericht bietet eine vollständige Rückverfolgbarkeit darüber, was, wer, wann ein Produkt geprüft wurde und welche Daten zu den Inspektionseinstellungen vorliegen. Die vollständige Inspektion kann dann jederzeit wiederholt werden.
Fazit
Die FDA verlangt 21 CFR Part 11 Einhaltung der Vorschriften für elektronische Aufzeichnungen. Im Laufe der Jahre hat sich dies von der einfachen Speicherung von Daten in einem Audit-Trail bis hin zur Sicherstellung der Richtigkeit der in Anwendungen und im Audit-Trail gespeicherten Daten ausgedehnt. Jede GlobalVision-Version wurde nach den strengsten Anforderungen an die Integrität pharmazeutischer Daten entwickelt und folgt zusätzlich einem vollständigen Softwareentwicklungszyklus, der sicherstellt, dass die funktionalen Anforderungen an Audit-Trails und Datenintegrität erfüllt, entworfen, entwickelt und getestet werden.
GlobalVision schützt vor Verpackungsfehlern, die sich auf Kunden auswirken, die Produkte außerhalb der Verkaufsregale kaufen. Das ist zweifellos von entscheidender Bedeutung. Integrierte Eventualitäten schützen jedoch auch die Organisationen, die die Software verwenden, indem sie sicherstellen, dass Daten niemals verloren gehen. Sie steht weiterhin allen zur Verfügung, die sie möglicherweise benötigen. Am wichtigsten ist, dass es völlig kompromisslos bleibt.


