Digitale Transformation für hochwertige pharmazeutische Verpackungen

Die vielen Komponenten der Lokalisierung
Alle Aspekte der Arzneimittelherstellung, einschließlich regulatorischer Angelegenheiten, Verpackung und Einhaltung der Vorschriften nach der Markteinführung, müssen den höchsten Qualitätskontrollstandards entsprechen, die von Behörden wie der FDA und der EMA festgelegt wurden. Da die Globalisierung die Marktgröße weiter erhöht, müssen Pharmaunternehmen die Lokalisierung jedes Produkts, das sie auf den Markt bringen, koordinieren. Sie müssen sicherstellen, dass ihre Produkte in mehreren Sprachen kommuniziert und zur Verfügung gestellt werden und gleichzeitig die Richtlinien und Compliance-Anforderungen aller Regionen, in denen sie tätig sind, einhalten. Neben Übersetzungen umfasst die Lokalisierung auch die Anpassung von Farbpräferenzen, Maßeinheiten, Datumsformaten, Grafiken und anderen Elementen, um den unterschiedlichen Märkten gerecht zu werden. In der Pharmaindustrie fallen in jeder Phase des Produktlebenszyklus mehr Informationen an als in jedem anderen Marktsegment. Rechtliche Unterlagen, Prospekte, Kartons, Beilagen und alle anderen Inhalte müssen so entwickelt werden, dass sie den besonderen Anforderungen eines bestimmten geografischen Gebiets entsprechen. Dies stellt die Aufsichtsbehörden vor Herausforderungen, wenn es darum geht, die Richtigkeit der Inhalte in jeder Phase des Arbeitsablaufs sicherzustellen. Darüber hinaus ist es aufgrund der Geschwindigkeit, mit der neue Medikamente auf den Markt gebracht werden müssen, schwierig, sicherzustellen, dass bei der Anpassung der Inhalte an lokale Märkte keine Fehler gemacht wurden. Dadurch wird ein Prozess, bei dem die Fehlerquote ohnehin gering ist, enorm kompliziert, da eine fehlerhafte Lokalisierung zu potenziellen rechtlichen Problemen und Umsatzeinbußen auf ausländischen Märkten führen kann.

Verpackungsfehler sind auf dem globalen Pharmamarkt zu einer der Hauptursachen für Rückrufe geworden, da die Produktverpackungen ständig an die Lokalisierungsanforderungen angepasst werden. Von Rechtschreibfehlern, die bei der Übersetzung von Fremdsprachen auftreten, bis hin zu Grafikfehlern — das Risiko, dass ein Verpackungsfehler übersehen wird, ist hoch. Da der Markt immer größer wird und Pharmaunternehmen immer dynamischer werden, wird die regulatorische Arbeitsbelastung immer komplexer und schwieriger zu bewältigen. Fachkräfte sind oft sehr gefragt und das Angebot ist knapp, was in Bereichen wie Compliance, Grafikmanagement und Etikettierung Spielraum für Fehler schafft. Um diesem zunehmenden Trend gerecht zu werden, führen immer mehr Unternehmen digitale Lösungen für verschiedene Aspekte des pharmazeutischen Workflows ein.
Einsatz von Technologie für den Betrieb in großem Maßstab
Eine der größten Herausforderungen für Fachleute aus den Bereichen Qualitätskontrolle und Regulierung ist die Menge an Daten, die sie täglich verwalten müssen. Regulatorische Angelegenheiten spielen eine entscheidende Rolle, da sie als Bindeglied zwischen Gesundheitsbehörden und verschiedenen Abteilungen innerhalb des Unternehmens dienen, um sicherzustellen, dass alle gesammelten Daten ordnungsgemäß transkribiert werden, um das Medikament herzustellen und zu vermarkten. Von der Zulassung eines neuen Produkts bis hin zur Sicherstellung, dass die korrekten FDA-Richtlinien bei der Etikettierung in Bezug auf Inhalt und Formatierung eingehalten werden, ist die Abteilung für regulatorische Angelegenheiten an vielen verschiedenen Aspekten der Produktion beteiligt. Darüber hinaus müssen in jeder Phase des Workflows zur Dateierstellung Überprüfungen durchgeführt werden, um sicherzustellen, dass die Informationen korrekt sind und den Genehmigungen entsprechen.

Eine wichtige Methode zur effektiven Bewältigung der zunehmenden Arbeitsbelastung infolge der Globalisierung besteht darin, Technologielösungen zu nutzen, die es ermöglichen, regulatorische Angelegenheiten in der Pharmaindustrie in großem Umfang abzuwickeln. Wenn es um das Korrekturlesen geht, sind manuelle Prozesse angesichts des Umfangs und der Geschwindigkeit, in der Produkte geliefert werden müssen, nicht mehr durchführbar. A) digital Qualitätskontrollsystem kann zur Überprüfung der Inhaltsgenauigkeit digitaler Dateien und gedruckter Verpackungsmaterialien verwendet werden, sodass kein manuelles Korrekturlesen und die damit verbundenen Ineffizienzen erforderlich sind.
Digitales Korrekturlesen für den pharmazeutischen Workflow
Automatisiertes Korrekturlesen kann in jeder Phase des pharmazeutischen Workflows implementiert werden, um sicherzustellen, dass keine Fehler verursacht oder eingeführt wurden. Zunächst werden die Produkt- und Arzneimittelvorschriften den Aufsichtsbehörden vorgelegt, die die Informationen dann in Informationsdokumenten zusammenfassen, die dann von der zuständigen Aufsichtsbehörde überprüft werden. Die Einführung eines digitalen Qualitätskontrollsystems in dieser Phase würde sicherstellen, dass alle Dokumente fehlerfrei sind und für interne Überarbeitungen und behördliche Einreichungen korrekt sind, da textlastige Dokumente automatisch Zeichen für Zeichen überprüft werden. In der Phase der Grafikerstellung können Grafikdateien automatisch überprüft werden, um sicherzustellen, dass bei der Dateierstellung keine Fehler aufgetreten sind. Zu diesen Fehlern gehören häufig Konformitätsfehler wie Logofehler, falsche Informationen und Barcodefehler. Die digitalen Inspektionen können während der Bearbeitung der Dateien fortgesetzt werden, um sicherzustellen, dass keine unbeabsichtigten Fehler hinzugefügt wurden.

Es ist unerlässlich, dass die Inhalte in jeder Phase des Prozesses in allen Abteilungen korrekt bleiben. Eine digitale Korrekturleselösung hilft auch dabei, den Überblick über Versionsänderungen zwischen den Abteilungen zu behalten, wodurch lange Genehmigungszyklen und Markteinführungszeiten reduziert werden. In der letzten Phase kann die digitale Qualitätskontrollsoftware die genehmigten Dateien vor dem Druck automatisch mit den Proofs von Lieferanten vergleichen und so sicherstellen, dass die Produkte mit einer völlig fehlerfreien Verpackung auf den Markt kommen. Digitale Systeme verbessern die Gesamteffizienz des pharmazeutischen Verpackungsablaufs weiter, da sie die Revisionszyklen verkürzen und Fehler früher im Prozess erkennen, egal wie klein die Fehler sind.
„Um Rückrufaktionen zu verhindern und eine gute Etikettierungsqualität zu gewährleisten, die den Vorschriften entspricht, können Sie das nicht alleine bewältigen. Sie benötigen ein Tool wie GlobalVision, um nicht nur schneller, sondern auch sicherer zu sein.“
Caroline Sell
Manager für regulatorische Angelegenheiten Merz Pharmaceuticals
Eine weitere Herausforderung für regulatorische Fachkräfte in der Pharmaindustrie ist die Verwaltung von Inhalten in Fremdsprachen. Da Medizinprodukte weiterhin ihren Weg in ausländische Märkte finden, müssen Verpackungen, textlastige Beilagen und IFUs in verschiedene Sprachen übersetzt werden. Übersetzungen werden häufig an externe Unternehmen ausgelagert, die bis zu 2000 Wörter pro Tag übersetzen können, sodass ein erhebliches Fehlerpotenzial besteht. Technologielösungen können dabei helfen, dies effektiv zu bewältigen, indem sie das Dokumentenmanagement, die Versionskontrolle und die Qualitätssicherung durch automatisiertes Korrekturlesen, das viele Fremdsprachen unterstützt, verbessern.
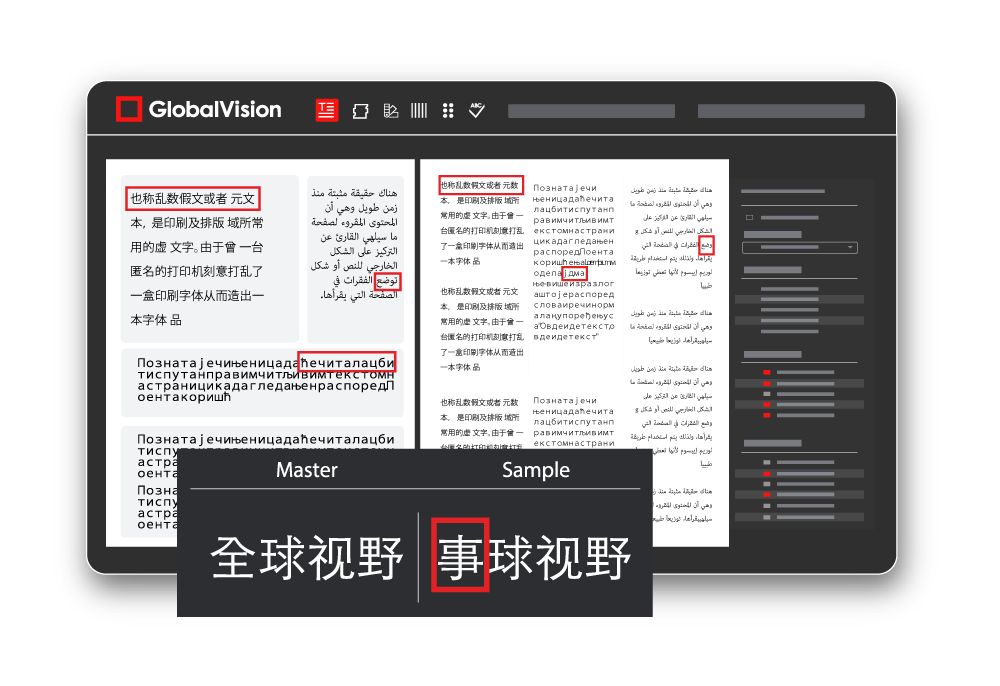
In der Pharmaindustrie sind Richtlinien zur Einhaltung von Vorschriften und zur Datenintegrität unerlässlich. Rohdaten sollten für den Fall von Untersuchungen aufbewahrt werden. Digitale Tools zur Qualitätskontrolle verwenden Audit-Trails, um alle Aktivitäten nachzuverfolgen und so die Einhaltung von Vorschriften wie ISO-Zertifizierungen, 21 CFR Part 11 und Anhang 11 sicherzustellen. Audit-Trails sind wichtig, da sie der Schlüssel zur Aufrechterhaltung der Datenintegrität sind, indem sie alle Aktivitäten, einschließlich Inspektionen und Berichte, verfolgen. Umfassende Inspektionsberichte tragen zum Schutz der Datenintegrität bei, indem sie eine vollständige Rückverfolgbarkeit darüber ermöglichen, wer ein Produkt geprüft hat und welche Ergebnisse die Inspektion hatte. Diese Berichte verfolgen und überprüfen alle festgestellten Unterschiede zwischen den Dateien und stellen so sicher, dass die richtigen Änderungen vorgenommen werden.
Fazit
Es besteht kein Zweifel, dass digitale Lösungen eine Versicherung gegen potenziell katastrophale Fehler wie fehlende Dezimalstellen in Dosierungsangaben sind. Der Wert, den sie Pharmaunternehmen bieten, geht weit über den Verzicht auf manuelles Korrekturlesen hinaus. Da sich die Art der regulatorischen Standards ständig weiterentwickelt, wächst auch die Notwendigkeit, technologische Lösungen wie die automatische Qualitätskontrolle effektiv umzusetzen. Diese technologischen Innovationen verbessern nicht nur die Prozesse zwischen den Teams, sondern fördern auch die funktionsübergreifende Zusammenarbeit und geben Pharmaunternehmen die Tools an die Hand, die sie benötigen, um auf globaler Ebene agieren zu können.


